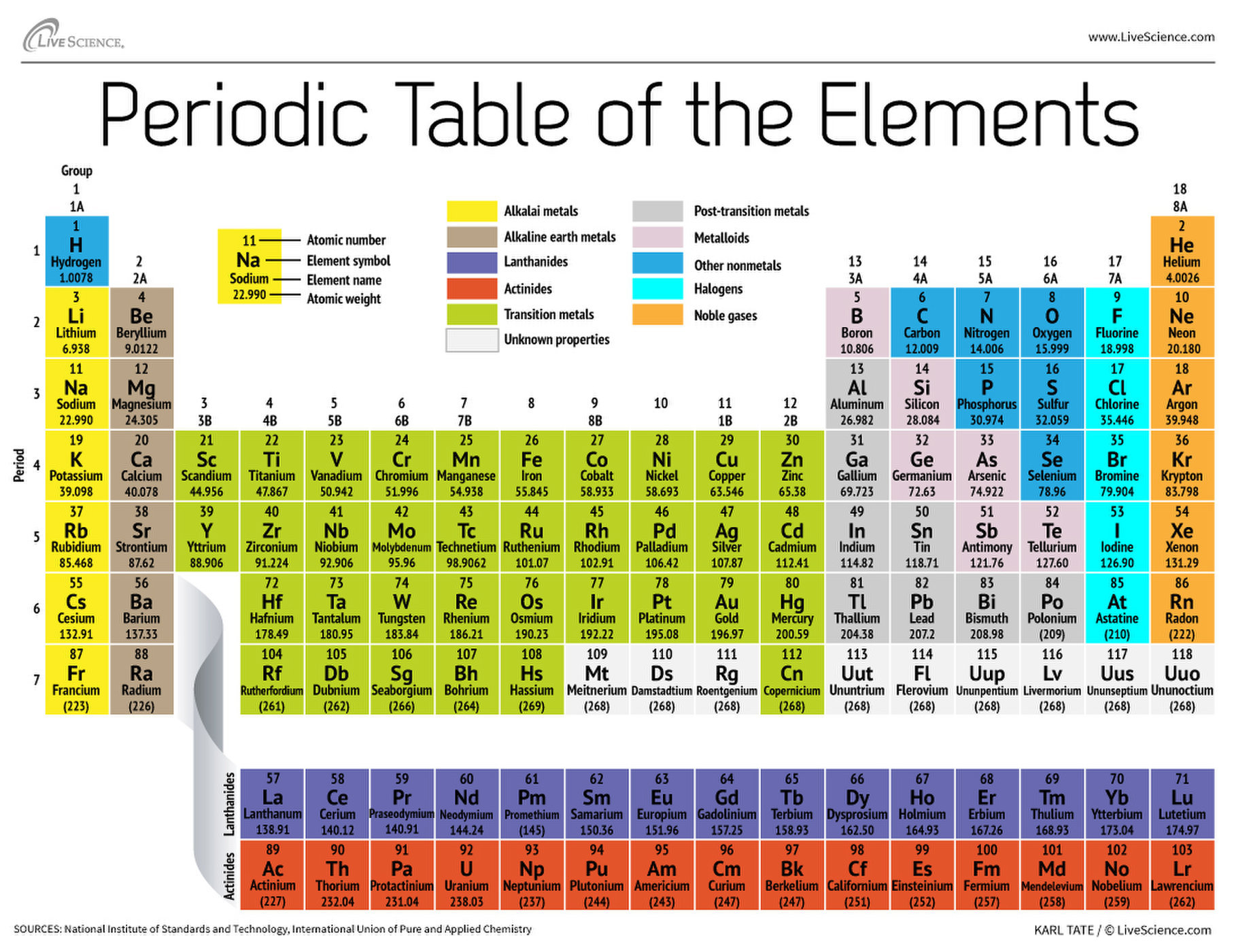
Astăzi, după 150 de ani, chimiştii cunosc 118 elemente şi încă folosesc tabelul periodic al elementelor. Acesta începe cu cel mai simplu atom, apoi grupează restul elementelor în funcţie de numărul atomic, adică numărul de protoni pe care îl conţine fiecare. Cu câteva excepţii, ordinea elementelor corespunde cu o creştere în masă de la un atom la altul, scrie Live Science.
Credit: Karl Tate
Sistemul periodic al elementelor are şapte rânduri şi 18 coloane. Fiecare rând reprezintă o perioadă; numărul periodic al unui element indică câte niveluri din energia sa este ocupată cu electroni. Spre exemplu, sodiul se află în a treia perioadă, ceea ce înseamnă că atomul de sodiu are electroni pe primele 3 niveluri de energie (configuraţia electronică a sodiului este 1s2 2s2 2p6 3s1). Următoarele rânduri/perioade sunt mai lungi întrucât este nevoie de mai mulţi electroni pentru a umple învelişurile externe, mai complexe ale atomului.
Coloanele tabelului periodic reprezintă grupe sau familii de elemente. Elementele dintr-un grup arată şi se comportă în mod similar, pentru că au acelaşi număr de electroni în învelişul extern – faţa pe care o arată lumii. Spre exemplu, coloana a 18-a, în dreapta extremă a tabelului, este formată din elemente cu un înveliş electronic complet, ceea ce înseamnă că participă foarte rar la reacţii chimice.
Elementele mai sunt şi clasificate ca metal sau nemetal, dar graniţa nu este clară. De obicei, elementele metalice sunt buni conducători de electricitate şi căldură. Subgrupurile metalelor sunt bazate pe caracteristici şi proprietăţi chimice similare.
Metale alcaline: acestea formează o mare parte din prima grupă, prima coloană a tabelului periodic. Suficient de moi pentru a fi tăiate cu un cuţit, grupul începe cu litiul (Li) şi se termină cu franciul (Fr). Sunt extrem de reactive, putând chiar să explodeze la contactul cu apa. Hidrogenul, cu singurul său electron, aflat în aceeaşi coloană, dar este considerat nemetal.
Metale alcalino-pământoase: acestea formează a doua grupă, de la beriliu (Be) până la radiu (Ra). Fiecare element are doi electroni în învelişul extern, ceea ce îi face suficient de reactivi. De aceea, în natură apar de obicei în molecule. Totuşi, nu sunt atât de reactive precum metalele alcaline şi produc mai puţină căldură decât elementele din grupa 1.
Lantanide: a treia grupă este prea lungă pentru a intra în a treia coloană, de aceea se află în primul rând de jos. Începe cu lantanul (La) şi se termină cu luteţiul (Lu). Acestea au o culoare argintie şi se degradează la contactul cu aerul.
Actinidele: aflate chiar sub rândul lantanidelor, acestea încep cu actiniul (Ac) şi se termină cu lawrenciul (Lr). Dintre acestea, doar thoriul (Th) şi uraniul (U) se găsesc natural pe Pământ în cantităţi substanţiale şi toate sunt radioactive. Lantanidele şi actinidele formează un grup din tabelul periodic care împreună se cheamă metale de tranziţie internă.
Metale de tranziţie: întorcându-ne la corpul principal al sistemului periodic al elementelor, restul grupei 3 până la grupa 12 sunt metale de tranziţie. Dure dar maleabile, strălucitoare cu o bună cunductivitate, aceste elemente sunt cele la care te gândeşti când auzi cuvântul metal, precum fierul, argintul, aurul şi platina.
Metale de post-tranziţie: spre lumea nemetalelor, caracteristicile nu sunt atât de bine definite între grupurile elementelor dispuse vertical. Metalele de post-tranziţie sunt aluminiul (Al), galiul (Ga), indiul (In), thaliul (Tl), staniul (Sn), plumbul (Pb) şi bismutul (Bi). Acestea sunt răspândite din grupa 13 până în grupa 17. Acestea au caracteristicile clasice ale metalelor de tranziţie, dar tind să fie mai moi şi să fie conducătoare mai slabe decât alte metale de tranziţie.
Metaloidele: acestea sunt borul (B), siliciul (Si), germaniul (Ge), arsenicul (As), stibiul (Sb), telurul (Te) şi poloniul (Po). Formează o scară care reprezintă o trecere graduală de la metale la nemetale. Aceste elemente din sistemul periodic se comportă câteodacă ca semiconductori (B, Si, Ge), fiind numite şi semimetale.
Nemetalele: toate elementele de la partea din dreapta-sus a scării plus hidrogenul (H), care intră în componenţa grupei 1. Acestea sunt carbonul (C), azotul (N), fosforul (P), oxigenul (O), sulful (S) şi seleniul (Se).
Halogenii: aceştia reprezintă grupa 17, de la fluor (F) la astatin (At). Sunt de asemenea nemetale şi sunt extrem de reactive. Tind să formeze molecule cu metalele alcaline pentru a produce diferite săruri. Spre exemplu, sarea de bucătărie este „mariajul” dintre sodiu (metal alcalin) şi clor (halogen).
Gazele nobile: fără culoare, fără miros şi aproape complet nonreactive. Acestea sunt gazele nobile inerte care formează grupa 18 din tabelul periodic al elementelor.
Vă recomandăm să citiţi şi următoarele articole:
Există un număr limită al elementelor chimice din Tabelul Periodic?
Opt elemente chimice foarte utile, dar mai puţin cunoscute – VIDEO
Chimistul care a scris ISTORIE şi a ajuns să fie o victima propriului succes
Top 10 aspecte mai puţin cunoscute despre tabelul periodic