Până la acest studiu, heliul era acel element care nu interacţionează cu nimic, indiferent de condiţiile la care era supus, notează Science Alert.
Acest principiu al chimiei a fost depăşit de cercetători care au creat un compus stabil de heliu şi sodiu. Ivan Popov, cercetător la Universitatea din Utah, care a luat parte la acest studiu, dezvăluie: „chimia se schimbă atunci când aplici presiuni mari, iar acest lucru poate fi realizat în interiorul Pământului sau pe alte planete precum Saturn”.
De ce este importantă această descoperire?
Heliul este al doilea element ca răspândire în Univers, iar cunoaşterea modului de comportare în interacţiunea cu alte elemente poate oferi informaţii esenţiale cu privire la compoziţia interiorului planetelor şi, de asemenea, formarea şi evoluţia acestora.
Face parte dintr-un grup de şase elemente numite gaze nobile. Unele dintre acestea au arătat semne de reacţii în condiţii extreme, astfel acest grup se poate împărţi în două: kripton, xenon şi radon fiind considerate mai reactive, iar argonul, neonul şi heliul mai puţin reactive.
Cercetătorii au mai putut să amestece heliul cu alte elemente, dar niciodată nu au reuşit să creeze un compus stabil. Unul dintre cele mai recurente exemple al intercţiunii heliului cu alte elemente are în vedere forţele van der Waals – forţe de atracţie sau respingere care nu necesită legături ionice sau covalente – unde este implicată cedarea de electroni, respectiv punerea în comun de electroni.
Lipsa de reactivitate a heliului se datorează configuraţiei electronice, singurul înveliş electronic pe care îl are este complet, astfel nu este loc de punere în comun de electroni cu alţi atomi. Aceast principiu are în vedere doar condiţiile de pe suprafaţa Terrei, la alte presiuni şi temperaturi comportamentul atomilor este susceptibil la schimbare.
Astfel, fiind foarte răspândit în Univers, condiţiile acestea pot exista dincolo de suprafaţa Terrei, chiar şi la presiunile din interiorul planetei noastre.
„Rezultatele au fost total neaşteptate”
Cercetătorii au folosit un model computerizat care poate prezice că, sub presiuni extreme, un compus de sodiu şi heliu a putut fi format. Apoi aceştia au creat fizic compusul nemaiîntâlnit, Na2He – supunând atomii de sodiu şi heliu la o presiune de 1,1 milioane de atmosfere.
Alex Boldyrev, care a participat la acest studiu, menţionează că „rezultatele au fost total neaşteptate”, luându-le doi ani să convingă comunitatea ştiinţifică de validitatea rezultatelor.
De asemenea, curios este faptul că nu există legături chimice care să ţină compusul laolaltă. Xiao Dong, de la Universitatea Nankai din China, care a participat la acest studiu, dezvăluie că „acest compus pe care l-am descoperit este foarte ciudat: atomii de heliu nu formează legături chimice, dar totuşi prezenţa lor schimbă în mod fundamental interacţiile chimice între atomii de sodiu, forţând electronii să se localizeze în interiorul vidurilor cubice ale structurii”.
Mai jos este structura compusului, cu atomii de sodiu (violet), heliul (verde) şi electronii (roşu) din vidurile cubice:
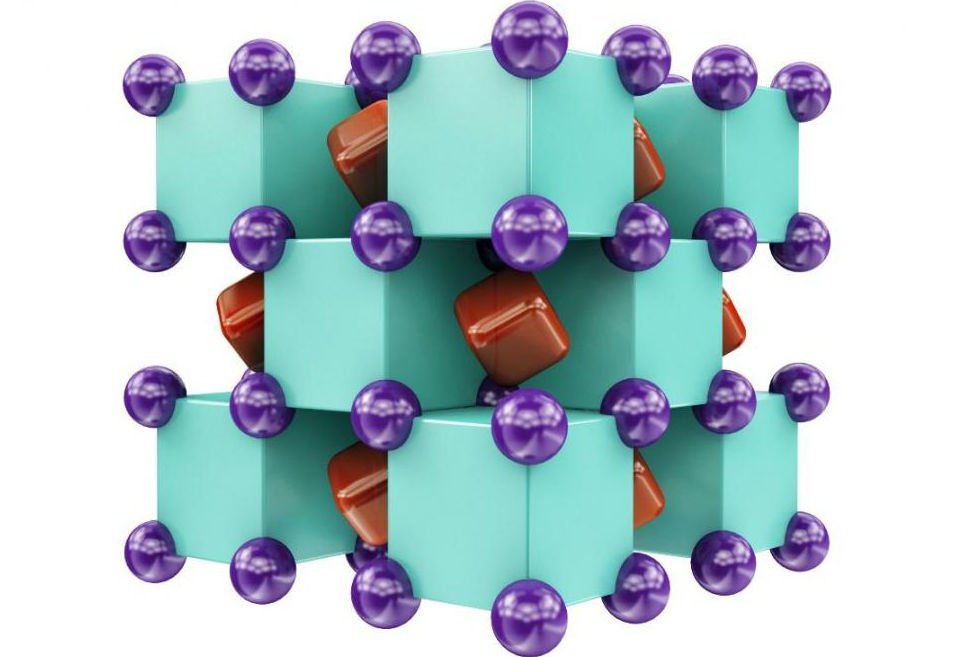
Această descoperire este esenţială pentru modul în care privim interacţiunile chimice, arătând că şi cel mai nereactiv element, dându-i condiţiile necesare, poate forma compuşi cu alte elemente.
Vă recomandăm să citiţi şi următoarele articole:
Cinci invenţii din domeniul chimiei care au făcut posibilă lumea aşa cum o cunoaştem astăzi
Zece accidente ştiinţifice care au dus la mari descoperiri
L-a prezentat pentru prima dată în urmă cu 146 de ani. Acum îl învăţăm cu toţii la ora de chimie